
随着化妆品行业对高效、安全、稳定传递活性成分的需求激增,超高压脂质体包裹技术(High-Pressure Liposome Encapsulation Technology)逐渐成为研究热点。该技术通过施加超高压力(通常为100-200 MPa),结合动态高压均质或微射流技术,实现活性成分的高效负载与缓释。
脂质体(Liposomes)是由磷脂和胆固醇等类脂质分子自组装形成的双分子层囊泡结构,直径通常在25-1000nm之间。其生物学定义可追溯至1961年,英国血液学家Alec D. Bangham首次提出这一概念。磷脂分子具有亲水头部和疏水尾部,在水中自发形成双层膜结构,包裹水相内核,形成类似细胞膜的封闭囊泡。
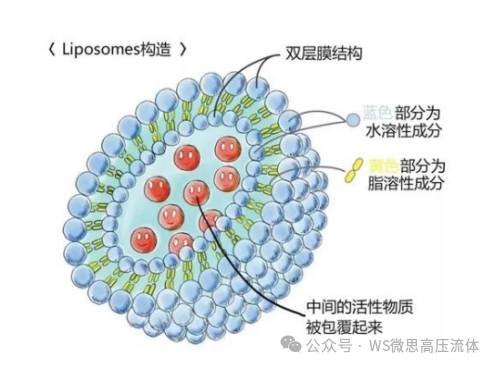
图2 脂质体结构图
水合渗透机制
磷脂分子增强角质层水合作用,使角质细胞膨胀率提升40-60%,细胞间隙扩大至50-80nm。
水溶性成分(如透明质酸)通过扩大的间隙渗透,脂溶性成分(如辅酶Q10)经扩散和毛细作用进入真皮层。
膜融合递送机制
脂质体磷脂双层与细胞膜通过疏水键-范德华力发生融合,形成瞬时通道(直径2-5nm)。
包裹物(如维生素C)直接注入细胞质,生物利用度提升2.3倍。
完整内吞机制
巨噬细胞通过网格蛋白依赖的内吞摄取脂质体(粒径100-200nm最优),形成内吞体。
酸性环境下(pH 5.0-5.5)脂质体膜破裂,释放药物至溶酶体,实现靶向递送。
材料准备与薄膜形成
将磷脂(如卵磷脂)、胆固醇、药物及抗氧化剂(如VE)溶于有机溶剂(如乙醇),通过旋转蒸发(45℃、真空度-0.09 MPa)除去溶剂,形成均匀的脂质薄膜。

图3 脂质薄膜微观视图
水化与粗悬液制备
加入缓冲液(如0.01 mol/L磷酸盐缓冲液,pH 7.4),在45℃水浴中旋转水合30分钟,
得到脂质体粗悬液。
高压均质处理
将粗悬液通过高压微射流均质机处理,关键参数包括:
压力:通常控制在80-160 MPa(11,600-23,200 PSI)。压力过大会破坏脂质体结构,过小则粒径控制不佳。
循环次数:3-5次。循环次数增加可提升包封率,但过多会导致机械破坏。
案例分享:
| 领域 | 应用场景 | 案例与技术优势 |
|---|---|---|
| 制药 | 抗肿瘤药物递送 | 多柔比星脂质体:粒径120nm,延长血液循环时间3倍,心脏毒性降低60% |
| 化妆品 | 美白精华 | 熊果苷脂质体:透皮率提升40%,稳定性提高8倍 |
| 食品 | 功能饮料营养强化 | ω-3脂肪酸脂质体:生物利用度提升55%,掩蔽鱼腥味 |
| 农业 | 农药缓释剂 | 阿维菌素脂质体:持效期延长至28天,减少用药量30% |
1.高活性成分的精准负载
美白配方:将超高压脂质体用于包裹四氢姜黄素(易氧化)与烟酰胺(pH敏感),高压环境隔绝氧气并维持中性条件,包封率可达85%以上;
抗衰配方:包裹胜肽(易降解)与麦角硫因,通过高压均质实现纳米级分散(粒径<100 nm),提升皮肤渗透率。
2.复合功能脂质体的开发
抗氧化+保湿协同:
内水相:透明质酸+依克多因(抗炎修复);
外油相:辛酸/癸酸甘油三酯+维生素E(双重锁水);
3.高压处理后形成“三明治”结构,兼具即刻补水与长效抗氧化效果。
4.解决传统痛点
刺激性问题:超高压脂质体包裹果酸或A醇,降低局部浓度梯度,减少皮肤泛红;
溶解难题:高压辅助溶解白藜芦醇(难溶于水),再通过脂质体包埋实现水基体系稳定。
微思纳米均质机在脂质体制备中具有更广泛的应用,包括纳米药物的开发、基因递送系统的构建、以及化妆品和食品领域的应用。微思纳米均质机在脂质体应用方面可能朝着智能化、自动化方向发展,通过集成传感器和控制系统实现更精准的工艺控制,推动脂质体技术的创新和发展。